
La mastocytose est une maladie définie par une prolifération et une accumulation anormale de mastocytes. Dans sa classification consensuelle, l’OMS distingue la mastocytose cutanée (accumulation limitée à la peau) et la mastocytose systémique. Cette dernière (forme la plus courante) consiste en une accumulation dans les autres tissus comme la moelle osseuse ou bien dans d’autres organes extracutanés. Les patients les plus touchés sont des adultes, bien que la maladie puisse survenir à tout âge. Qu’est-ce que c’est que la mastocytose systémique ? Comment se développe-t-elle ?
Mastocytose systémique : description
La mastocytose systémique désigne un groupe de maladies rares caractérisées par une prolifération et une accumulation excessive de mastocytes. Ce phénomène se déroule dans les tissus de la moelle osseuse et dans d’autres organes du corps. Ce sont le foie, la rate, les ganglions lymphatiques et le tractus gastro-intestinal. L’affection, rare, touche principalement les adultes. Selon une statistique, une personne sur 150 000 développe la mastocytose systémique.
Par ailleurs, il en existe cinq différents types, qui diffèrent en fonction de leur gravité et de leurs manifestations. Ce sont :
- La mastocytose systémique indolente (asymptomatique et lente),
- La mastocytose systémique fumante,
- La mastocytose systémique associée à une tumeur hématologique (dans ce cas, il n’y a pas de mastocytes),
- La mastocytose systémique agressive,
- La leucémie à mastocytes.
Les types légers de cette maladie incluent la forme lente et fumante, généralement associés à un pronostic favorable. Les trois derniers types de la mastocytose systémique (agressive, associée à un néoplasme hématologique et leucémie à mastocytes) comptent parmi les types les plus graves. Dans ces cas, on note une réduction importante de l’espérance de vie.
Mastocytose systémique : causes
Les causes de la mastocytose systémique n’ont pas encore été clairement reconnues. Cependant, la prolifération incontrôlée des mastocytes en serait la principale cause déclenchant les symptômes. Elle est souvent associée à la génétique et à la sécrétion d’histamine.
Les mastocytes
Les mastocytes sont un ensemble de cellules qui appartiennent au système immunitaire. Ils ont alors pour principal rôle de défendre l’organisme contre les agents infectieux ainsi que d’autres types de menaces. En présence des bactéries ou virus, ils commencent à libérer une substance dans les vaisseaux sanguins : l’histamine. Cette dernière est l’une des causes des symptômes de la prolifération des mastocytes dans la moelle osseuse.
Par ailleurs, les mastocytes destinés à résider dans les tissus tels que la peau, les poumons ou l’intestin proviennent généralement de la moelle osseuse. Ils circulent dans le sang en tant que cellules précurseurs CD34+. Ensuite, ils traversent les cellules endothéliales et se déposent dans ces tissus précités. Là, ils se différencient et deviennent matures tout en formant des granules de sécrétion (dégranulation) sous l’influence de plusieurs facteurs. Il s’agit notamment du Stem Cell Factor (SCF).
La mutation génétique
Dans la plupart des cas, la prolifération excessive des mastocytes est également due à une mutation génétique acquise. Autrement dit, elle n’a pas été héritée d’un parent. Elle affecte particulièrement le gène c-kit qui produit une protéine appelée KIT ou CD117. Cette dernière fonctionne comme un récepteur du Stem Cell Factor, qui est un facteur capable de stimuler la prolifération et l’activation des mastocytes.
En fait, les mutations qui affectent le gène c-kit sont capables de provoquer une activation spontanée du récepteur. Cela entraîne également une prolifération consécutive des mastocytes. Dans la mastocytose, la mutation du gène c-kit D816V représente plus de 90 % de toutes les mutations décrites. Elle entraîne le remplacement de l’acide aspartique (D) par l’acide valine (V) à la position numéro 816 de la protéine. Aussi, elle est fréquemment identifiée chez les patients atteints de mastocytose systémique.
Contrairement aux mastocytes normaux, les mastocytes de la mastocytose systémique expriment normalement les gènes appelés CD25 et CD2. Des cellules plus immatures pourraient également exprimer des antigènes supplémentaires.
Les facteurs de risque
De nombreux facteurs induisent la libération des substances contenues dans les granules, avec l’apparition de signes cliniques et de symptômes. Ce sont par exemple :
- Les traumatismes,
- Les changements thermiques,
- Les piqûres d’insectes,
- L’exercice physique,
- Le stress et anxiété ;
- L’alimentation (alcool, fromages, boissons, aliments fermentés, fruits, œufs, poissons, conserves).
Les médicaments sont également des facteurs de risque courants. Par exemple, on peut citer l’acide acétylsalicylique (aspirine) et autres AINS (anti- inflammatoires), la codéine, les antibiotiques et les produits de contraste iodés.
Mastocytose systémique : symptômes
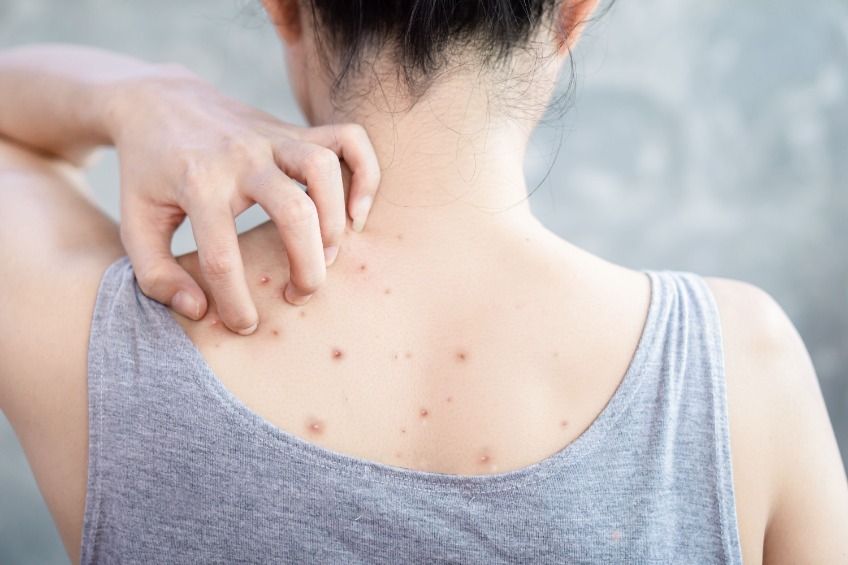
Les symptômes de la mastocytose systémique sont dus au fait que les tissus sont occupés par la masse de mastocytes. Ceux-ci réagissent par la fibrose et la libération de substances actives agissant au niveau local et au niveau systémique. Les manifestations cliniques observées peuvent être aggravées par les facteurs de risque susmentionnés. Selon l’organe atteint, on distingue respectivement la mastocytose hématologique, digestive et osseuse. Des démangeaisons dues à une urticaire peuvent également survenir.
Symptômes hématologiques
La prolifération des mastocytes dans la moelle osseuse est fréquente. En excès, ces cellules remplacent celles sanguines normales, comme les globules rouges, provoquant une anémie. Dans les 50 % des cas, on note une accumulation de mastocytes également dans la rate avec élargissement de l’organe (splénomégalie). L’atteinte des ganglions lymphatiques profonds provoque une augmentation de leur taille et l’apparition de douleurs abdominales dues à la compression d’autres organes. On peut également noter une hypertrophie du foie (hépatomégalie) et un ictère subséquent. Tout cela provoque un sentiment d’apathie.
Par ailleurs, le sous-type, leucémie à mastocytes est une manifestation courante. C’est une affection caractérisée par une augmentation significative des mastocytes atypiques et immatures dans le sang ou la moelle osseuse. Cela implique des dommages possibles aux organes internes où les mastocytes s’accumulent. Des signes et symptômes graves tels que des saignements dus à un manque de plaquettes peuvent entraîner la mort. Ce sont là des complications de la mastocytose systémique.
Manifestations osseuses
Il s’agit de formes latentes souvent retrouvées à la suite d’examens radiographiques. Ceux-ci sont souvent pratiqués sur des patients qui se plaignent de douleurs osseuses ou qui ont subi des fractures. Les lésions osseuses d’accumulation de mastocytes peuvent être localisées ou diffuses. Elles peuvent à la longue entraîner une ostéoporose (complication de la mastocytose).
Troubles digestifs
Les symptômes gastro-intestinaux de la mastocytose sont provoqués par une libération excessive de médiateurs par les granules ainsi qu’à une infiltration locale. Les symptômes les plus courants sont les nausées, les vomissements, les douleurs abdominales, la malabsorption (qui entraîne une perte de poids).
Autres signes cliniques
Les autres signes typiques peuvent être des fractures pathologiques secondaires à une ostéolyse (spontanée). Une thrombocytopénie et des infections récurrentes secondaires à une insuffisance médullaire peuvent survenir. L’ascite est plus fréquente en cas de mastocytose associée à une autre anomalie hématologique. Aussi, elle est de mauvais pronostic et difficile à contrôler. Une hypertension portale peut également survenir, mais elle peut être gérée par un shunt porta-cave (prothèse).
En outre, la mastocytose systémique peut se caractériser par l’apparition des symptômes suivants :
- Les palpitations (rythme cardiaque irrégulier),
- Les bouffées de chaleur,
- Les étourdissements,
- Une hypotension avec un malaise général ou des évanouissements,
- Les maux de tête.
Ces symptômes apparaissent brutalement sous forme de crises d’une durée de 15 à 30 minutes. Après cela, ils peuvent disparaître progressivement pour réapparaître plus tard.
Mastocytose systémique : diagnostic
Pour établir le bon diagnostic de mastocytose systémique, les 5 tests suivants doivent être effectués dans l’ordre.
Numération sanguine complète
C’est le décompte de toutes les cellules et les autres éléments présents dans le sang. La numération sanguine complète nécessite le prélèvement d’un échantillon de sang dans une veine du bras et son analyse minutieuse. Si, à la fin des tests, un taux de cellules sanguines étrangement bas ressort, cela pourrait signifier qu’il y a une présence excessive de mastocytes dans la moelle osseuse. Une partie de cette substance produit les cellules sanguines.
Analyse pour la détection des taux sanguins de tryptase
La tryptase est une enzyme présente uniquement à l’intérieur des mastocytes, plus précisément dans les granules. Par conséquent, une quantité élevée de tryptase dans le sang d’un individu n’est pas bon signe. Cela signifie qu’il y a certainement un nombre élevé de mastocytes en circulation. La quantification des concentrations de tryptase est réalisée avec un test sanguin spécial.
Échographie abdominale
Il s’agit d’un examen radiologique non invasif, qui fournit des images claires des organes internes du corps. On peut le faire pour les patients suspects de mastocytose systémique (numération sanguine complète et analyse positive du niveau de tryptase). Ainsi, cela va permettre de détecter si le foie et la rate sont hypertrophiés.
L’absorptiométrie biénergétique à rayons X (DEXA ou DXA)
La DEXA un test aux rayons X, qui permet de mesurer les niveaux de calcium dans les os d’un individu. Dans le cas d’une mastocytose systémique, ces organes sont pauvres en calcium et sujets à l’ostéoporose. En effet, ils subissent une infestation par un nombre excessif de mastocytes, qui produisent des substances corrosives.
Prélèvement et analyse de moelle osseuse (biopsie)
La moelle osseuse se trouve dans les zones les plus internes de certains os. Par conséquent, le prélèvement d’un échantillon nécessite une seringue avec une très longue aiguille et une petite anesthésie locale. Cette dernière est à pratiquer là où le spécialiste a l’intention d’insérer l’aiguille. Une fois la quantité nécessaire de moelle prélevée, les cellules qu’elle contient sont analysées. Dans la moelle osseuse d’un individu atteint de mastocytose systémique, on observe une grande quantité de mastocytes.
Autres examens
Le diagnostic peut toutefois nécessiter d’autres examens supplémentaires.
La scintigraphie osseuse
Cet examen peut montrer la présence de signes d’ostéoporose, d’ostéosclérose ou de foyers d’ostéolyse. Dans la plupart des cas, les lésions ostéolytiques sont petites et ne s’accompagnent pas de symptômes cliniques. Dans d’autres cas, des fractures pathologiques spontanées peuvent survenir. Récemment, on a pu conclure que 9 % des cas d’ostéoporose chez les hommes sont secondaires à la mastocytose.
L’immunohistochimie et l’examen histologique
La moelle osseuse est l’organe systémique le plus fréquemment atteint. Un examen histologique et chimique peut mettre en évidence une infiltration de mastocytes dans les tissus.
Pour ce faire, on utilise des colorations appropriées, telles que la coloration de Giemsa, la coloration au bleu de toluidine et les colorations anti-tryptase.
De plus, les mastocytes peuvent être rendus visibles grâce à la réaction de la chloroacétate estérase, une enzyme qui n’est pas exclusive aux mastocytes. Chez certains patients, le pourcentage de mastocytes dans l’aspirat de moelle osseuse (échantillon de l’aspiration) est inférieur à 5 % et parfois même inférieur à 1 %. Un pourcentage supérieur à 20 % est presque un diagnostic de leucémie à mastocytes.
Mastocytose systémique : traitement

Actuellement, il n’existe aucun traitement curatif de la mastocytose. Les patients atteints de mastocytose indolente ont généralement une progression lente dans le temps et doivent être étroitement surveillés. Voici les options de traitement disponibles.
Traitement par IFN-alpha-2b et prednisolone
Chez les patients atteints de mastocytose systémique et de lésions osseuses importantes, un plan serait une combinaison de l’IFN-alpha-2b et de la prednisolone. Le traitement par prednisolone débute pendant quelques jours, on ajoute l’IFN-alpha2b à une certaine dose. Pendant les premiers jours du traitement par IFN, il faudra surveiller les patients à l’hôpital. Après quelques semaines, la dose journalière d’IFN peut être augmentée et la prednisolone réduite à une dose d’entretien, voire arrêtée.
Chez les victimes atteintes d’ostéoporose sévère et de fractures, l’administration d’IFN-alpha-2b sans glucocorticoïdes semble préférable. En fait, ces derniers peuvent provoquer des effets secondaires. Par contre, chez celles qui y répondent bien, on peut poursuivre le traitement jusqu’à l’apparition de signes, de symptômes de toxicité ou d’effets secondaires.
Dans une revue de la littérature disponible, certains chercheurs ont décrit 14 patients atteints de mastocytose agressive traités par IFN-alpha avec ou sans prednisolone. Parmi ceux-ci, 21,4 % ont présenté une réponse majeure avec disparition des symptômes. Cinq patients ont eu une réponse partielle et 42,9 % des patients n’ont pas répondu. Les taux de réponse étaient similaires chez ceux qui ont reçu l’association avec des corticoïdes que chez ceux qui n’en ont pas reçu.
Lorsque l’IFN ne suffit pas à contrôler l’affection, on peut essayer les cytostatiques susceptibles d’arrêter la prolifération des mastocytes. Comme exemple, on peut mentionner la daunorubicine, la cladribine, l’hydroxyurée et la cytosine arabinoside.
Chimiothérapie d’induction et de consolidation ou greffe osseuse
Si la situation le permet et qu’il y a une plus grande réponse à la chimiothérapie d’induction, certains patients peuvent être candidats à une greffe de moelle osseuse. Si cette dernière ne peut pas être appliquée, les personnes en rémission doivent recevoir un traitement de consolidation.
Pendant le traitement de chimiothérapie, la surveillance sera basée sur une série de paramètres. Ce sont :
- Enzymes hépatiques élevées,
- Calcium sanguin élevé,
- Diminution de l’hémoglobine.
Sur la base de ces données, on parle de réponse clinique pure lorsqu’il n’y a qu’une amélioration de ces paramètres. Quant à la réponse complète, elle est valable lorsque ceux-ci sont rendus normaux. Aucune réponse signifie que le contraire se produit (les paramètres ne reviennent pas à la normale).
Biologie moléculaire
On peut également faire recours à une approche de la biologie moléculaire qui consiste en une administration de médicaments comme l’Imatinib. Ils sont efficaces dans les cas où il y a certaines mutations, comme ceux du gène c-kit.
Médicaments complémentaires
Tous les patients atteints de mastocytose agressive reçoivent des antagonistes de l’histamine anti-H1 et anti-H2 ou bien de la prednisolone. Il convient de noter que cela doit se faire avant la chimio, car les médiateurs des mastocytes peuvent provoquer des symptômes importants. Certaines victimes présentent des symptômes sévères et récurrents associés aux médiateurs et sont à risque de développer un choc cardiovasculaire. Dans ce cas, on recommande que l’épinéphrine soit disponible pour l’auto-administration si nécessaire.
Le traitement des troubles digestifs quant à lui est variable. Les anticholinergiques peuvent apporter un certain soulagement. Le sodium de cromolyn par voie orale peut aussi être utile pour gérer les symptômes touchant l’abdomen. Les glucocorticoïdes systémiques sont également efficaces chez les patients souffrant de malabsorption sévère. Il en est de même dans les cas d’ascite exsudative.
Traitement de la forme sévère : la leucémie à mastocytes
Il n’existe pas de traitement efficace pour les patients atteints de cette forme. Même la chimiothérapie conventionnelle ne produit pas de réponse durable chez ces personnes. C’est pourquoi des schémas thérapeutiques agressifs, tels que ceux utilisés dans la leucémie myéloïde aiguë, sont utilisés. Toutefois, si un donneur est disponible et qu’une rémission a été obtenue après la chimiothérapie, il est possible de procéder à une greffe de moelle osseuse.
Traitement des hémopathies malignes
Chez environ 15 à 30 % des patients atteints de mastocytose systémique, on peut observer une hémopathie maligne associée. Cela inclut les syndromes myéloprolifératifs, les syndromes myélodysplasiques ou la leucémie myéloïde aiguë. Il est parfois difficile de faire la distinction entre une hémopathie maligne associée et une mastocytose.
L’option thérapeutique la plus recommandée consiste à planifier le traitement de l’hémopathie maligne comme s’il n’y avait pas de mastocytose systémique. Aussi, il faudra opter pour une thérapie pour la mastocytose systémique comme si l’autre pathologie n’existait pas. Par la suite, le professionnel de santé adapte le traitement.




